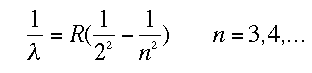En un principi, no, i per això es van crear models d'àtoms, per a entendre com es va formar la matèria. Primer Thomson va designar una definició per a dos nous conceptes: El electró (amb càrrega negativa) i el protó (amb càrrega positiva). Rutherford va pensar un model d'àtom tipus planetari, on els àtoms orbitaven al voltant d'un nucli. Aquest model va estar molt bé perque no ficaven els àtoms en el nucli com si fora un "pudding". Però d'altra banda, el model tenia unes órbites el·líptiques, on finalment els àtoms xocarien amb el nucli, tampoc va explicar amb el seu model els espectres (que eren ben coneguts en aquella època), llavors es va haver de descartar aquesta teoria. Rutherford també va suggerir l'existència d'altres partícules nuclears, de masa pràcticament la mateixa que la del protó i sense càrrega. Va ser Chadwick en 1932 qui va descobrir el neutró bombardejant átoms de Be (Beril·li) amb partícule
s alfa.
Balmer, anys després, va estudiar les línies de l'espectre d'hidrògen, on per casualitat, després de fer molts càlculs, va predir amb una fòrmula on ixirien les ratlles de l'espectre.
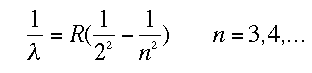
La R es la constant de Rydberg. Les fòrmules de Paschen i Lyman eren molt paregudes a les de Balmer, però Lyman en lloc de ficar un 2, va ficar un 1 i Paschen un 3.
Bohr, va ser el aprenent de Rutherford, va crear un model en el que els electrons orbitaven al voltant del nucli, de forma ondulatòria, fent un cercle però amb ondes totalment definides, on el punt inicial coincideix amb el punt final. La long. de ona es pot calcular amb l'equació anterior, la de Balmer.